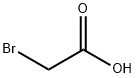
| Kemijske lastnosti |
BELA DO SVETLO RUMENA KRISTALNA MASA |
| Uporabe |
Organska sinteza, odstranjevanje citrusov pri obiranju. |
| Uporabe |
Bromoocetna kislina se uporablja v organski sintezi in kot alkilirno sredstvo. Uporablja se tudi kot biokemikalija za raziskave proteomike. Je pomembna surovina in intermediat, ki se uporablja v organski sintezi, farmacevtskih izdelkih, barvilih in agrokemikalij. |
| Uporabe |
Bromoocetna kislina se uporablja predvsem zaN-terminalna bromoacilacija peptidov, vezanih na smolo.
Uporablja se lahko tudi:Sintetizirati (Z)-2-(ciklookt-4-en-1-iloksi)ocetna kislina.
Sintetizirati -bromo-fenilacetamid.
Za pretvorbo aromatskih tiosemikarbazonov v tiazolilhidrazone.
|
| Splošni opis |
Vodna raztopina. |
| Reakcije zraka in vode |
Vodotopno. |
| Profil reaktivnosti |
Karboksilne kisline, kot je bromoocetna kislina, oddajajo vodikove ione, če je prisotna baza, ki jih sprejema. Na ta način reagirajo z vsemi bazami, tako organskimi (na primer amini) kot anorganskimi. Njihove reakcije z bazami, imenovane "nevtralizacije", spremlja razvoj znatnih količin toplote. Nevtralizacija med kislino in bazo proizvaja vodo in sol. Karboksilne kisline s šestimi ali manj ogljikovimi atomi so prosto ali zmerno topne v vodi; tisti z več kot šestimi ogljiki so rahlo topni v vodi. Topna karboksilna kislina do neke mere disociira v vodi, da nastanejo vodikovi ioni. pH raztopin karboksilnih kislin je zato manjši od 7.0. Številne netopne karboksilne kisline hitro reagirajo z vodnimi raztopinami, ki vsebujejo kemično bazo, in se raztopijo, ko nevtralizacija ustvari topno sol. Karboksilne kisline v vodni raztopini in tekoče ali staljene karboksilne kisline lahko reagirajo z aktivnimi kovinami, da tvorijo plinasti vodik in kovinsko sol. Takšne reakcije načeloma potekajo tudi pri trdnih karboksilnih kislinah, vendar so počasne, če trdna kislina ostane suha. Tudi "netopne" karboksilne kisline lahko absorbirajo dovolj vode iz zraka in se dovolj raztopijo v bromoocetni kislini, da razjedajo ali raztopijo železne, jeklene in aluminijaste dele in posode. Karboksilne kisline, tako kot druge kisline, reagirajo s cianidnimi solmi in tvorijo plinasti vodikov cianid. Reakcija je počasnejša pri suhih, trdnih karboksilnih kislinah. Netopne karboksilne kisline reagirajo z raztopinami cianidov in povzročijo sproščanje plinastega vodikovega cianida. Vnetljivi in/ali strupeni plini in toplota nastajajo pri reakciji karboksilnih kislin z diazo spojinami, ditiokarbamati, izocianati, merkaptani, nitridi in sulfidi. Karboksilne kisline, zlasti v vodni raztopini, reagirajo tudi s sulfiti, nitriti, tiosulfati (da nastanejo H2S in SO3), ditioniti (SO2), da nastanejo vnetljivi in/ali strupeni plini in toplota. Njihova reakcija s karbonati in bikarbonati ustvarja neškodljiv plin (ogljikov dioksid), vendar še vedno toploto. Tako kot druge organske spojine lahko tudi karboksilne kisline oksidiramo z močnimi oksidanti in reduciramo z močnimi redukcijskimi sredstvi. Te reakcije ustvarjajo toploto. Možna je široka paleta izdelkov. Tako kot druge kisline lahko karboksilne kisline sprožijo reakcije polimerizacije; tako kot druge kisline pogosto katalizirajo (povečajo hitrost) kemične reakcije. |
| Nevarnost |
Močno draži kožo in tkivo. |
| Nevarnost za zdravje |
STRUPENO; vdihavanje, zaužitje ali stik (koža, oči) s hlapi, prahom ali snovjo lahko povzroči hude poškodbe, opekline ali smrt. Stik s staljeno snovjo lahko povzroči hude opekline kože in oči. Reakcija z vodo ali vlažnim zrakom bo sproščala strupene, jedke ali vnetljive pline. Reakcija z vodo lahko povzroči veliko toplote, ki poveča koncentracijo hlapov v zraku. Ogenj bo proizvedel dražeče, jedke in/ali strupene pline. Odtekanje vode za gašenje požara ali vode za redčenje je lahko jedko in/ali strupeno in povzroči onesnaženje. |
| Nevarnost požara |
Gorljiv material: lahko gori, vendar se ne vname takoj. Snov bo reagirala z vodo (nekatere burno), pri čemer bodo sproščeni vnetljivi, strupeni ali jedki plini in odtok. Pri segrevanju lahko hlapi tvorijo eksplozivne mešanice z zrakom: nevarnost eksplozije v zaprtih prostorih, na prostem in v kanalizaciji. Večina hlapov je težjih od zraka. Širijo se po tleh in zbirajo v nizkih ali zaprtih območjih (kanalizacija, kleti, rezervoarji). Hlapi lahko potujejo do vira vžiga in se vrnejo nazaj. V stiku s kovinami se lahko razvije vnetljiv vodikov plin. Posode lahko eksplodirajo pri segrevanju ali če so onesnažene z vodo. |
| Vnetljivost in eksplozivnost |
Ni vnetljivo |
| Varnostni profil |
Strup z zaužitjem, intraperitonealno in intravensko. Dražilno in jedko za kožo in sluznico. Sporočeni podatki o mutaciji. Pri segrevanju do razgradnje oddaja strupene hlape Br-. Glej tudi BROMIDI. |
| Metode čiščenja |
Kristalizirajte bromoocetno kislino iz petroletra (b 40-60o). Njegovo raztopino v dietilnem etru spustimo skozi kolono aluminijevega oksida in eter uparimo pri sobni temperaturi v vakuumu. Najbolje ga je dobiti z destilacijo iz Claisenove posode (bučka, potopljena v oljno kopel), opremljene z izolirano Vigreuxovo kolono (str. 11), pri čemer se zbere frakcija b 108-110o/30 mm. Je občutljiv na svetlobo in vlago. [Natelson & Gottfried Org Synth Coll Vol III 381 1955, Beilstein 2 IV 526.] SOLEZEN in je DRAŽILEC kože. |