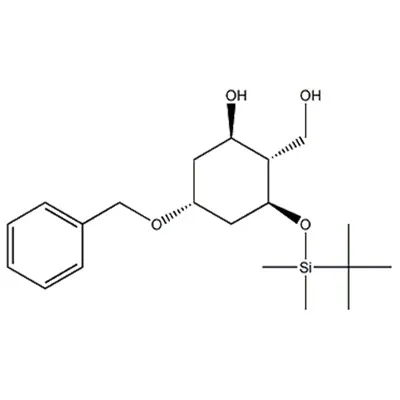
Predstavitev izdelka
| Tetrabutilamonijev bromid Osnovne informacije |
| Fizikalne in kemijske lastnosti Uporaba Uporabe pripravka Strupenost |
| Ime izdelka: | Tetrabutilamonijev bromid |
| sinonimi: | 1-Butanaminij, N,N,N-tributil-,bromid;1-Butanaminij,N,N,N-tributil-,bromid;n,n,n-tributil-1-butanaminiubromid; ALIQUAT(R) 100;IPC-TBA-BR;Tetrabutilazanijev bromid;Tetrabutilaminijev·bromid;Tetrabutilamonijev bromid, 99 %, za kromatografijo z ionskimi pari |
| CAS: | 1643-19-2 |
| MF: | C16H36BrN |
| MW: | 322.37 |
| EINECS: | 216-699-2 |
| Kategorije izdelkov: | organo amin halid; drugi izdelki; bistvene kemikalije amonijeve soli; rutinski reagenti; analitični reagenti amonijevih soli; elektrokemija; podporni elektroliti za elektrokemijo; anionska HPLC; reagenti za kromatografijo/CE; ionski par; reagent za ionski par; s - anionski; ionski par Reagenti - anionski koncentrat; kvartarne amonijeve soli; amonijevi bromidi (kvartarni); analitična kemija; HPLC reagenti ionskih parov za kisle vzorce; reagenti ionskih parov za HPLC; kvartarne amonijeve spojine; amonijeve, fosfonijeve, sulfonijeve soli (ionske tekočine); ionske Tekočine;Sintetična organska kemija;Amonijeve soli;Zelenejše alternative: kataliza;Katalizatorji faznega prenosa;Farmacevtski intermediati;1643-19-2;bc0001 |
| Mol datoteka: | 1643-19-2.mol |
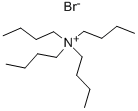 |
|
| Kemijske lastnosti tetrabutilamonijevega bromida |
| Tališče | 102-106 stopinj (osvetljeno) |
| Vrelišče | 102 stopinji |
| gostota | 1,039 g/ml pri 25 stopinjah |
| parni tlak | 0Pa pri 25 stopinjah |
| lomni količnik | n20/D 1.422 |
| Fp | 100 stopinj |
| skladiščna temp. | Hraniti pod +30 stopinjami. |
| topnost | H2O: 0.1 g/mL, bistro, brezbarvno |
| oblika | Kristalni prah |
| pka | 0[pri 20 stopinjah] |
| Specifična težnost | 1.007 |
| barva | Bela do rahlo smetanasta |
| Neprijeten vonj | Kot amin |
| PH | 3,5 do 7.0 (50 g/L, 25 stopinj) |
| Topnost v vodi | 600 g/L (20 ºC) |
| Občutljivo | Higroskopičen |
| λmaks | λ: 240 nm Amax: 0,04 λ: 250 nm Amax: 0,03 λ: 260 nm Amax: 0,02 λ: 500 nm Največ: 0,02 |
| BRN | 3570983 |
| Stabilnost: | Stabilen. Nezdružljivo z močnimi oksidanti. Zaščititi pred vlago. |
| InChIKey | JRMUNVKIHCOMHV-UHFFFAOYSA-M |
| LogP | 0.839 pri 25 stopinjah |
| Referenca baze podatkov CAS | 1643-19-2(referenca baze podatkov CAS) |
| NIST Chemistry Reference | Tetra-N-butilamonijev bromid (1643-19-2) |
| Sistem registra snovi EPA | Tetrabutilamonijev bromid (1643-19-2) |
| Varnostne informacije |
| Kode nevarnosti | Xi, Xn |
| Izjave o tveganju | 36/37/38-22 |
| Izjave o varnosti | 26-36-37/39 |
| WGK Nemčija | 3 |
| F | 3 |
| Opomba o nevarnosti | Dražilno |
| TSCA | ja |
| oznaka HS | 29239000 |
| Informacije o varnostnem listu |
| Ponudnik | Jezik |
|---|---|
| Tetrabutilamonijev bromid | angleščina |
| ACROS | angleščina |
| SigmaAldrich | angleščina |
| ALFA | angleščina |
| Uporaba in sinteza tetrabutilamonijevega bromida |
| Fizikalne in kemijske lastnosti | Tetrabutilamonijev bromid, znan tudi kot tetrabutilamonijev bromid. Bel kristal, raztopljen. 118 stopinj tališče. Topen v vodi, alkoholu, etru in acetonu, rahlo topen v benzenu.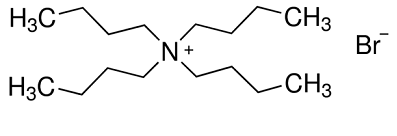 Slika 1: strukturna formula tetrabutilamonijevega bromida |
| Aplikacija | (1) Uporablja se kot reagent za analizo organske sinteze. (2) Tetrabutilamonijev bromid je tudi učinkovit katalizator faznega prenosa. Katalizator za fazni prenos, imenovan PTC, je sposoben prenesti vodno fazo (ali organsko fazo) v katalizator organske faze (ali vodne faze), ki lahko povzroči reakcijo med vodno fazo in organsko fazo katalizatorja. PTC ima funkcijo spreminjanja stopnje solvatacije ionov, povečanja aktivnosti ionske reakcije, pospeševanja hitrosti reakcije in tako naprej. Rešite problem preteklosti v dveh fazah reakcije je težko reagirati. Običajni katalizatorji faznega prenosa kvarterne amonijeve soli so: benzil trietilamonijev klorid, trioktil metil amonijev klorid, tetrametil amonijev bromid, tetrapropilamonijev klorid, tetrabutilamonijev bromid, tetrabutilamonijev jodid, benzil trietilamonijev bromid, trietil heksil bromid, oktil trietilamonijev bromid mide. Katalizator faznega prenosa se pogosto uporablja v organski sintezi: R2C za pripravo spojin (spojina tipa karbena), nadaljnjo pripravo ustreznih derivatov nitrila, izonitrila, halona, diklorometana, ciklopropana, hidroksi kislin in diazometana. Za reakcijo alkilacije, v primerjavi s tradicionalnimi metodami, da bi se izognili težkim pogojem suhega delovanja in visokemu izkoristku, se lahko uporablja tudi v redoks reakciji, hidrolizi estra, reakciji substitucije, reakciji kondenzacije, reakciji dodajanja, reakciji polimerizacije, reakciji dodajanja ogljika in izločanje reakcije itd. (3) Za intermediate organske sinteze katalizator faznega prenosa (4) Reagenti za ionske pare za sintezo bakampicilina, sultamicilinu podobnega. (5) Reagenti za kromatografijo ionskih parov, katalizator faznega prenosa. Bakampicilin, sultamicilin podobna sinteza. |
| Uporabe | Tetrabutilamonijev bromid (TBAB) je kvarterna amonijeva spojina. Je najpogosteje uporabljen katalizator faznega prenosa. Njegove mejne lastnosti so preučevali v primeru reakcij, ki jih sproži hidroksid. To lahko uporabimo pri razumevanju mehanizma reakcij faznega prenosa. Poroča se, da TBAB skrajša retenzijski čas in odstrani konične ostanke, tako da deluje kot reagent ionskega para med kromatografsko analizo kvarternih amonijevih spojin. V staljenem stanju se TBAB obnaša kot ionska tekočina, ki je obetavna zelena alternativa organskim topilom v organski sintezi. Določene so njegova molarna toplotna kapaciteta, entropija in funkcija proste energije. Nedavno je bil staljeni tetrabutilamonijev bromid (TBAB) uporabljen kot nizko toksičen in stroškovno učinkovit IL v številnih konstruktivnih sintetičnih transformacijah. Tetrabutilamonijev bromid (TBAB) se lahko uporablja v staljenem stanju v naslednjih postopkih: Sinteza (2S)-5-(3-fenil-2-ftalimidilpropanoilamino)izoftalne kisline. Sinteza z alkilom substituiranih pirolov v odsotnosti katalizatorja in organskega topila. Sinteza ditioacetalov iz acetalov s transtioacetalizacijo v okolju brez topil. Sinteza poliamidov (PA) s polimerizacijo tereftalne kisline in diizocianatov. Katalizirajte adicijo tiolov na konjugirane alkene. Dehidrokloriranje poli(vinilklorida). |
| priprava | Preparativne metode: na voljo je več metod za učinkovito pridobivanje kvarternega amonijevega iona. Pripravljeno z reakcijo tri-n-butilamina in n-butil bromida. |
| Toksičnost | Akutni oralni LD50 (miš): 590 mg/kg. Vdihavanje, zaužitje in stik s kožo strupeno za kožo, oči in draženje dihal. Več informacij iz urednika ChemicalBook Xiaonan (2015-09-16). |
| Kemijske lastnosti | beli kristali ali prah |
| Uporabe | Tetrabutilamonijev bromid se uporablja pri sintezi polimernih sončnih celic. Uporablja se tudi pri sintezi enokomponentnih elektrokemičnih celic, ki oddajajo zeleno svetlobo. |
| Opredelitev | ChEBI: Tetrabutilamonijev bromid je tetrabutilamonijeva sol z bromidom kot anionskim dvojnikom. Je organska bromidna sol in tetrabutilamonijeva sol. |
| ugodnosti | Tetrabutilamonijev bromid je okolju prijazna, nehlapna, negorljiva, nekorozivna, poceni, komercialno dostopna amonijeva sol z visoko toplotno in kemično stabilnostjo. V TBAB se lahko tetrabutilamonijeva sol raztopi tako v vodnih kot tudi v organskih topilih, kar pomaga pri transportu vodotopnih anionskih reaktantov v organsko fazo. Poleg tega je bil staljeni TBAB uporabljen tudi kot učinkovita ionska tekočina za izvajanje organskih transformacij v pogojih brez topil[1]. |
| Splošen opis | Tetrabutilamonijev bromid, kvarterna amonijeva spojina, ki se pogosto uporablja kot katalizator faznega prenosa. TBAB skrajša retenzijski čas in odstrani vrhove repov tako, da deluje kot reagent ionskega para med kromatografsko analizo kvarternih amonijevih spojin. V staljenem stanju se TBAB obnaša kot ionska tekočina, ki je obetavna zelena alternativa organskim topilom pri sintezi polimerov. |
| Vnetljivost in eksplozivnost | Ni razvrščeno |
| Metode čiščenja | Kristalizirajte sol iz *benzena (5 ml/g) pri 80o z dodajanjem vročega n-heksana (tri volumne) in pustite, da se ohladi. Posušite ga nad P2O5 ali Mg(ClO4)2 v vakuumu. Sol je zelo higroskopična. Lahko ga tudi kristaliziramo iz etil acetata ali suhega acetona z dodatkom dietiletra in sušimo v vakuumu pri 60o 2 dni. Kristaliziran je bil iz acetona z dodatkom dietiletra. Je tako higroskopičen, da je treba vse manipulacije izvajati v suhi škatli. Očistili smo ga z obarjanjem iz nasičene raztopine v suhem CCl4 ob dodatku cikloheksana ali s prekristalizacijo iz etil acetata, nato pa s segrevanjem v vakuumu na 75° v prisotnosti P2O5. [Symons et al. J Chem Soc, Faraday Trans 1 76 2251 1908.] Prav tako prekristalizira iz CH2Cl2/dietil etra in se posuši v vakuumskem eksikatorju nad P2O5. [Blau & Espenson J Am Chem Soc 108 1962 1986, Beilstein 4 IV 657.] |
| Reference | [1] Banik B, et al. S tetrabutilamonijevim bromidom (TBAB) katalizirana sinteza bioaktivnih heterociklov. Molekule, 2020; 25: 5918. |
| Izdelki in surovine za pripravo tetrabutilamonijevega bromida |
| Izdelki za pripravo | 1-BENZOTHIOPHENE-5-CARBOXYLIC ACID-->Albendazole-->Piperonyl aldehyde-->3-AMINOBIPHENYL-->5-Bromoindazole-->ETHYL 4-ETHOXYPHENYLACETATE-->H-GLY-AMC HBR-->1-Phenylcyclopentanecarboxylic acid-->3-PHENYLBENZYLAMINE-->4-PYRIDIN-2-YLISOXAZOL-5-AMINE-->cintofen-->FENOTHIOCARB-->(R)-(-)-2,2-Dimethyl-1,3-dioxolane-4-methanol-->Isocarbophos-->Venlafaxine hydrochloride-->1-BENZOTHIOPHENE-5-CARBONITRILE-->N-(4-THIOPHEN-2-YL-PHENYL)-ACETAMIDE-->Thianaphthene-2-carboxylic acid-->Myclobutanil-->alpha-butyl-alpha-phenyl-1H-imidazole-1-propiononitrile-->5-Bromobenzo[c]thiophene-->Olaquindox-->Sisthsne-->2-[2-(DIPHENYLPHOSPHINO)ETHYL]PYRIDINE-->Glyceryl monostearate-->1-(3-Aminopropyl)piperidine-->Phenyl vinyl sulfone-->6-Bromopurine-->Methyl 3,4,5-trimethoxybenzoate-->CYCLANILIDE-->2-(4-ETHOXYPHENYL)-2-METHYL PROPIONITRILE-->Levetiracetam-->4-Bromo-7-azaindole-->DIOCTYL ETHER-->1,1-Cyclopropanedicarboxylic acid dimethyl ester-->2 -phenyl-Hexanenitrile-->Zeolite-->Tetrabutylammonium hexafluorophosphate-->4-(tert-Butyl)benzyl mercaptan-->Tetrabutilamonijev borohidrid |
Priljubljena oznake: tetrabutilamonijev bromid, Kitajska tetrabutilamonijev bromid proizvajalci, dobavitelji, tovarna
Morda vam bo všeč tudi
Pošlji povpraševanje